Diversi tumori solidi profondi locali ed ad alto rischio metastatico, ad oggi sono difficilmente trattabili. Ad esempio i tumori profondi non possono essere trattati con terapie fotodinamiche (PDT) e fototermiche (PTT) in quanto non possono essere raggiunti dalla luce visibile o infrarossa, alla base di questi trattamenti.
Stiamo implementando una nuova terapia basata su un nano-sistema (NS) composto da nanocristalli multifunzionali bidimensionali che, attivato da Raggi-X a bassa energia (E<200 KeV), rilascia localmente oncoterapie non mutagene. I RX non sono quindi usati come agenti radioterapici per sradicare il cancro, ma permettono di raggiungere e visualizzare durante la terapia, tumori profondi che sono inaccessibili dalla luce visibile o nel vicino infrarosso. In particolare, le terapie attivate si basano sulla generazione locale di calore, specie reattive dell'ossigeno, agenti radiosensibilizzanti e induzione di morte cellulare per immunogenesi con l'esposizione o il rilascio di neo-antigeni per innescare una risposta immunitaria anti-cancro. Il progetto considera una gamma di tipi di cancro tra cui il cancro triplo negativo metastatico al seno, il carcinoma epatocellulare, il cancro colorettale e pancreatico.
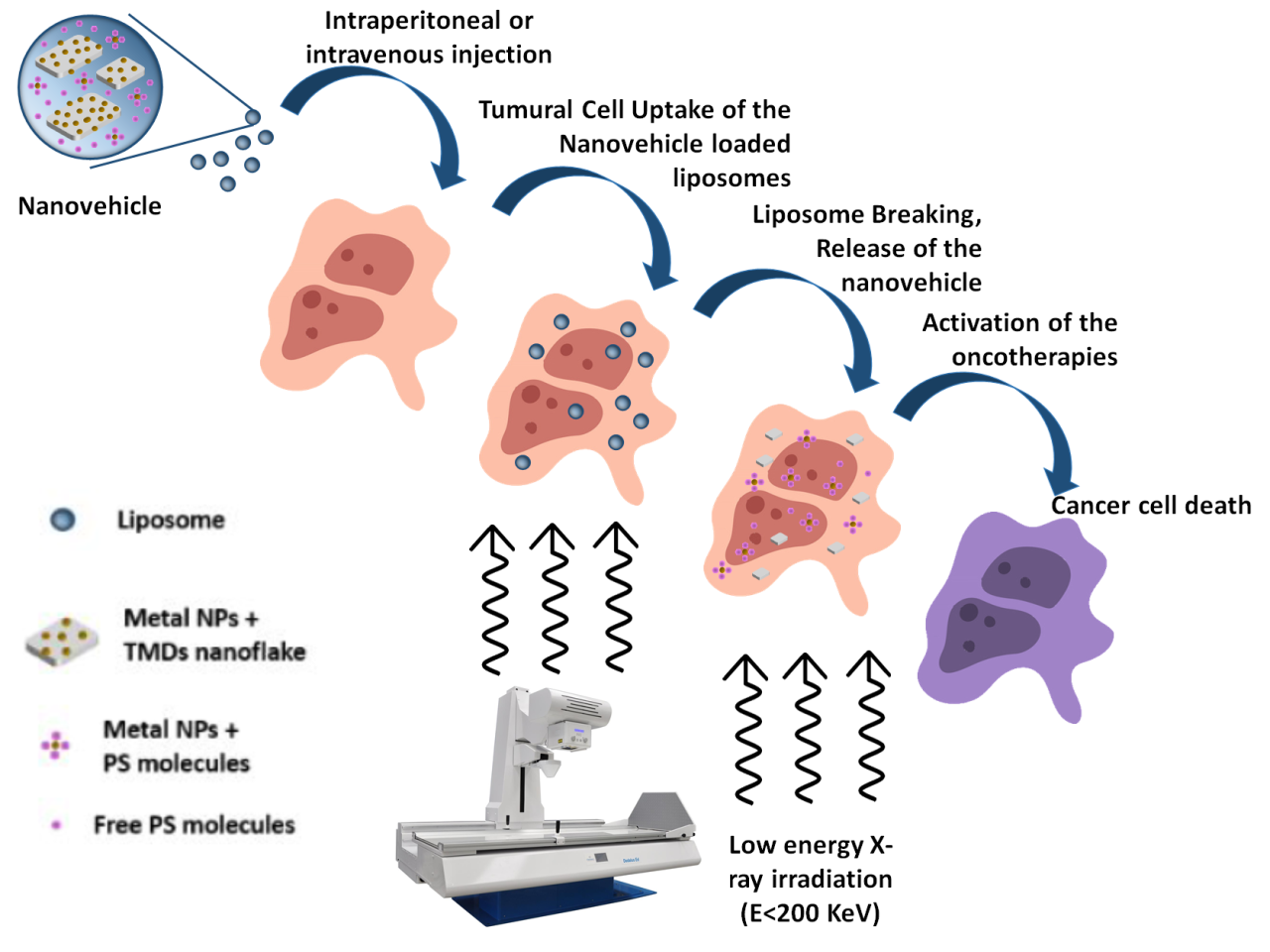 Principio di funzionamento
Principio di funzionamento
Il prodotto è un nanosistema (NS) costituito da nanocristalli bidimensionali biocompatibili (2D-NC) ad alto Z opportunamente funzionalizzati che, sotto irraggiamento X (RX) bassa energia, produce in sede locale e metastatica specie reattive dell'ossigeno, calore, immunoterapia e radiosensitizzazione. Il NS viene internalizzato in liposomi e successivamente inviato alle aree interessate dal tumore mediante iniezioni intraperitoneali o intravenose per targeting passivo o attivo. L'utilizzo di RX a bassa energia, riduce al minimo gli effetti collaterali associati alla radioterapia corrente, mentre l'assorbimento dei raggi X è notevolmente migliorato. Questo perché ad energie E<0.8-1 Mev il meccanismo di interazione predominante è l'effetto fotoelettrico con un coefficiente di assorbimento proporzionale a Z4/E3.
1) Per massimizzare l'assorbimento di energia per una conversione termica efficiente, il NS contiene nanoparticelle di metalli nobili (MENP) citocompatibili coniugate a 2D-NC. Le MENP agiscono come "nano-antenne" per l'assorbimento dei RX (nanofototermolisi); mentre i 2D-NC sono intermediari di aumento della temperatura. Le MENP mostrano anche un notevole contrasto ai RX permettendo la modalità teranostica.
2) I NS contengono un fotosensibilizzante che, sotto irraggiamento X, genera ossigeno singoletto.
3) Le MENP e 2D-NCS forniscono agenti radiosensibilizzanti che consentono una lisi localmente mediata dalle radiazioni delle cellule tumorali.
Ad oggi non esistono nanofarmaci antitumorali disponibili per il trattamento dei tumori umani nella clinica. Ciò è dovuto a: 1) Incertezza dell'efficacia terapeutica; 2) Problemi di sicurezza e biocompatibilità; 3) Ampia distribuzione nei tessuti non tumorali; 4) Limitata capacità di penetrazione dei tessuti a luce visibile e infrarossa per efficaci terapie quali la terapia fotodinamica (PDT) e fototermica (PTT); 5) Mancanza di effetti sinergici con le modalità terapeutiche esistenti come la chemioterapia, radioterapia (RT) e immunoterapia.
Il nostro approccio, che non prevede lo sviluppo di un vero e proprio nanofarmaco, ma di un nanodispositivo:
1) consoliderà i benefici della RT, PDT, PTT, nanofototermolisi ed immunoterapia con il vantaggio della penetrazione di tutto il corpo dei raggi X a bassa energia, minimizzando gli effetti collaterali negativi della RT;
2) consentirà trattamenti a lungo termine di PDT e PTT senza effetti collaterali e, soprattutto, senza limitazioni per i tipi di cancro in quanto non necessità di agenti terapeutici specifici come e.g. nel caso della chemioterapia.
Le applicazioni sono in campo oncoterapico di tumori solidi con alto rischio di metastasi, e.g.il tumore triplo negativo del seno ed il tumore del pancreas.
Il nuovo approccio, agisce anche con effetto abscopale, grazie all'uso di RX che inducono la morte cellulare immunogenica con la formazione o il rilascio di neo-antigeni per innescare una risposta immunitaria contro gli antigeni tumorali in siti distali.
Le MENP ed i 2D-NC possono avere anche applicazioni teranostiche per il monitoraggio della regressione tumorale senza la necessità di interventi separati o l’utilizzo di agenti di contrasto.
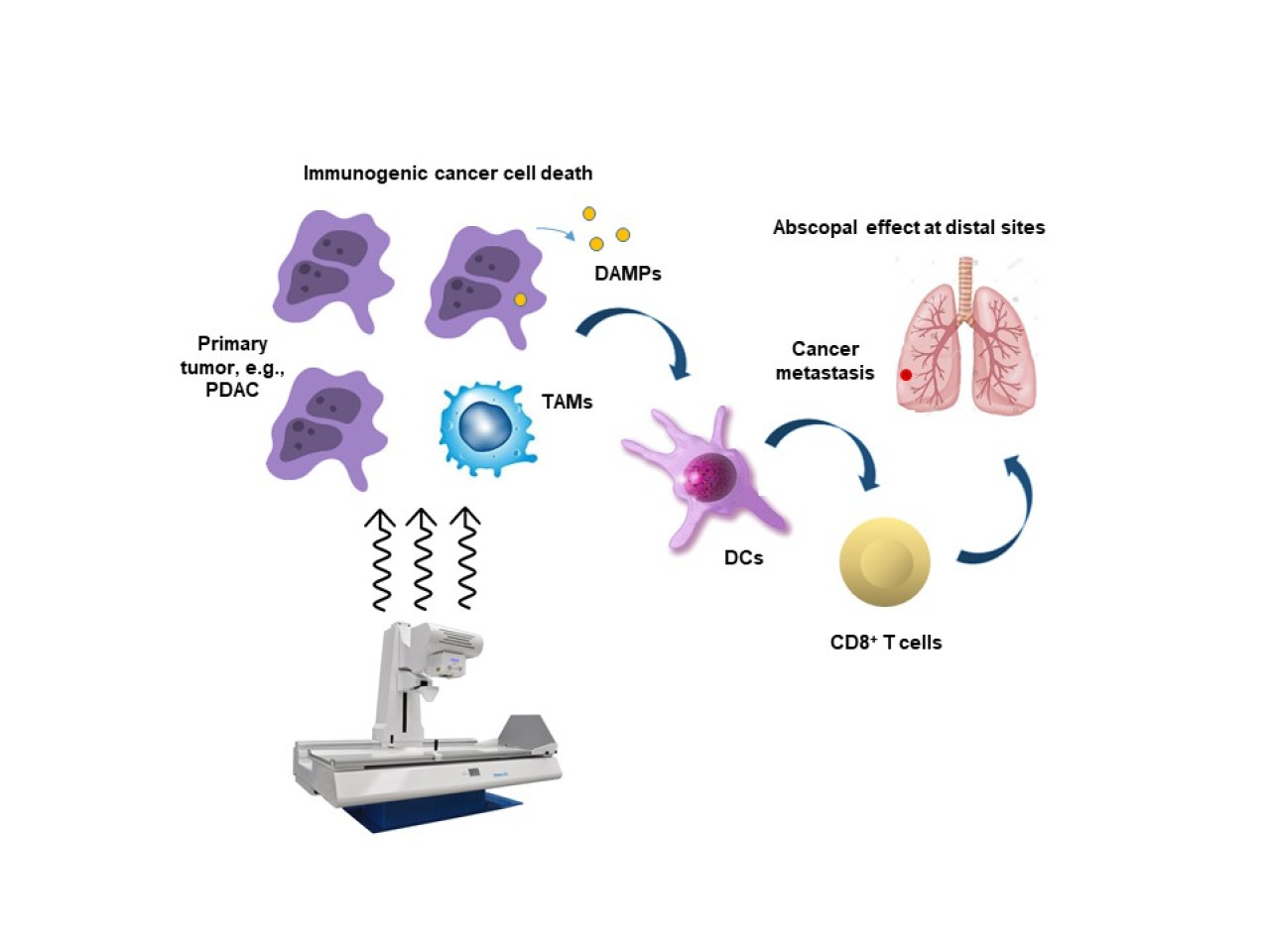 Effetto abscopale
Effetto abscopale
Terapia fotodinamica (PDT) mediante RX ad alta energia coadiuvata dalla presenza di nanofili (NWs) sia in vitro che in vivo per un adenocarcinoma polmonare
Una delle prime applicazioni è stata fatta su un adenocarcinoma polmonare utilizzando come cuore del nanosistema nanofili di SiC.
I nanofili, opportunamente funzionalizzati con molecole organiche in grado di rilasciare ossigeno singoletto se irradiate, sono stati inizialmente internalizzati a due diverse concentrazioni (100 micro gr/ml e 500 micro gr/ml) in cellule tumorali dell’adenocarcinoma polmonare (A549). In seguito i campioni sono stati sottoposti a radioterapia (6 Gy) per 20 sec. L’esperimento è stato ripetuto su cellule A549 senza NWs.
E’ stata dimostrata:
-in vitro, l’efficacia della presenza di NWs che, generando ROS sotto irraggiamento X, distrugge a 72 h le cellule cancerogene con una efficacia superiore massima di circa l’80% rispetto alla radioterapia senza NWs utilizzando concentrazioni di NWs di 500 micro gr/ml;
- in vivo su ratti Fisher, l’efficacia del trattamento radioterapico adiuvato da NWs è superiore del 40% circa alla radioterapia convenzionale senza NWs.
La nostra nuova tecnologia è più complessa rispetto ai semplici nanofili di SiC utilizzati in passato. Il nuovo nanosistema presenta vantaggi senza precedenti per portare la nanomedicina alla clinica, tra cui: 1) applicazione di NS multifunzionali per approcci terapeutici combinati e di imaging (teranostica); 2) attivazione di NS utilizzando RX a bassa energia, comunemente disponibili nella clinica; 3) penetrazione profonda dei tessuti per affrontare tumori situati negli organi interni e siti metastatici distali; 4) oncoterapia che combina la radioterapia e le varie modalità di fototerapia che portano alla morte cellulare immunogenica con rilascio di neoantigeni per evocare la risposta immunitaria contro il cancro.
Oncologi, radiologi, chimici, biologi, ingegneri chimici, fisici e scienziati dei materiali appartenenti a UNIPR; CNR-IMEM Parma; CNR-IMEM Trento; CNR-NANO Pisa; Karoliska Institute, Stockholm Sweden: Technion Institue, Haifa Israel, UNIVIGO Spain, Wigner Institute, Budapest Hungary.
Tutte le innovazioni saranno oggetto di brevetti, pubblicazioni scientifiche su riviste internazionali e di pubblicazione nei siti web dei partner interessati
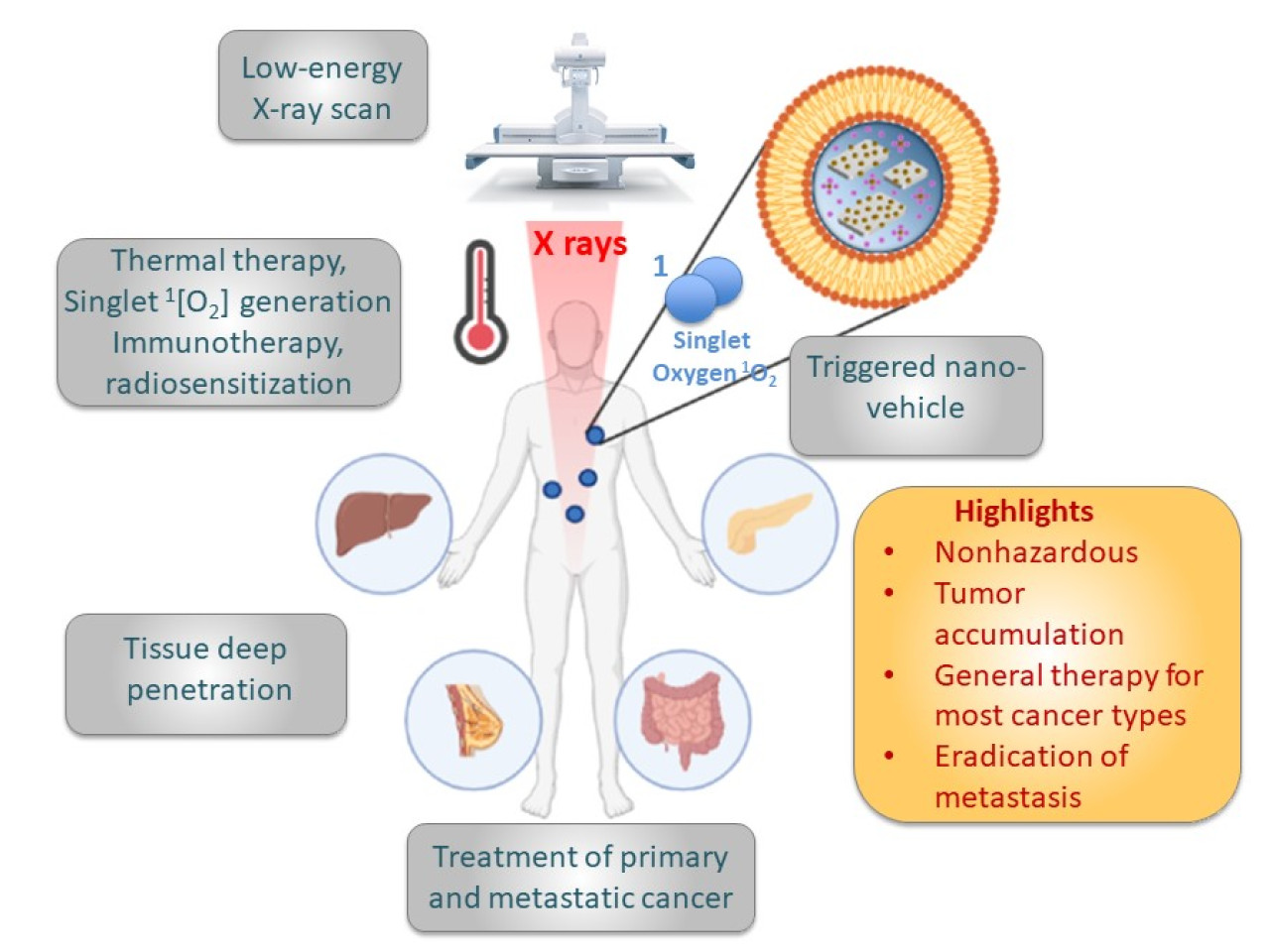 Possibili applicazioni
Possibili applicazioni

